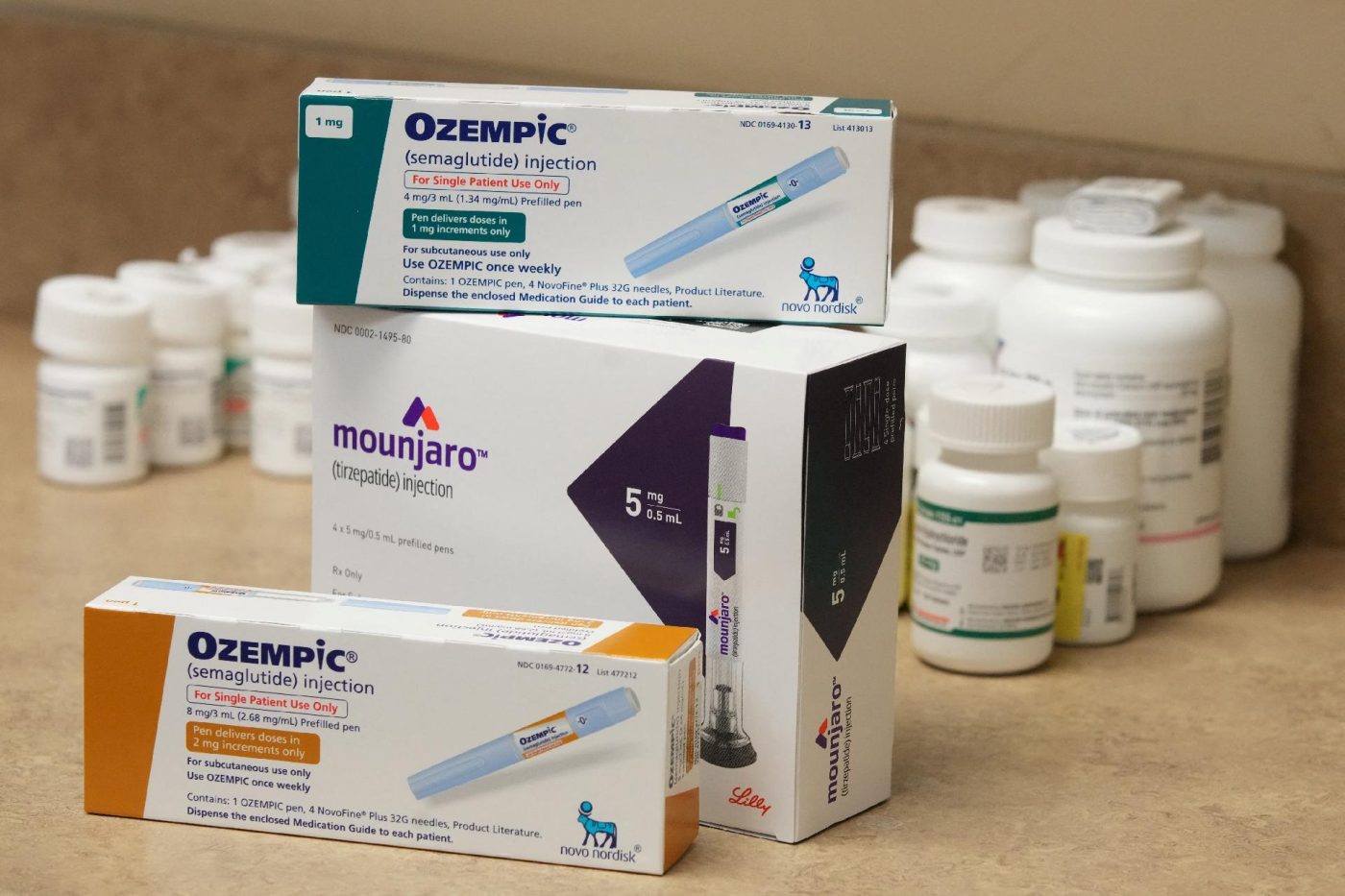
A Agência Nacional de Vigilância Sanitária anunciou, nesta segunda-feira (6), um conjunto de medidas para ampliar o controle sanitário sobre medicamentos injetáveis agonistas do receptor GLP-1, conhecidos como canetas emagrecedoras. A iniciativa busca reduzir riscos à saúde e coibir irregularidades na importação de insumos e na manipulação desses produtos.
Segundo a agência, há inconsistências entre o volume de insumos farmacêuticos importados e a demanda real do mercado. Apenas no segundo semestre de 2025, foram trazidos ao país 130 quilos de matéria-prima, quantidade suficiente para produzir cerca de 25 milhões de doses.
Em 2026, ações de fiscalização resultaram em 11 inspeções em farmácias de manipulação e empresas importadoras, com interdição de oito estabelecimentos por falhas técnicas e ausência de controle de qualidade.
De acordo com o diretor-presidente da Anvisa, Leandro Safatle, as medidas não têm como objetivo proibir a manipulação dos medicamentos, mas garantir segurança aos usuários. “Esse é um desafio regulatório não só para o Brasil, mas para as principais agências do mundo, essa situação do avanço do consumo de medicamentos derivados de GLP-1 e o avanço da manipulação em cima desses produtos”, afirmou.
A agência também aponta aumento de relatos de eventos adversos e do uso off label desses medicamentos, especialmente para emagrecimento sem indicação clínica. Em fevereiro, já havia sido emitido alerta para risco de pancreatite associado a esses produtos.
Entre os principais problemas identificados estão a produção sem receita individualizada, falhas de esterilização, deficiência no controle de qualidade e uso de insumos sem origem comprovada. Também foram detectadas irregularidades como uso indevido de nomes comerciais e comercialização de produtos sem registro.
Desde janeiro, a Anvisa publicou dez medidas proibindo a importação, comercialização e uso de itens irregulares que contêm substâncias como semaglutida, tirzepatida e liraglutida.
O plano de ação é estruturado em seis eixos. No campo regulatório, está prevista a revisão da Nota Técnica 200/2025, que trata de procedimentos para importação e manipulação desses insumos, além da atualização da RDC 67/2007, que estabelece boas práticas em farmácias de manipulação. A proposta também inclui o endurecimento de medidas cautelares, como a suspensão de autorizações de funcionamento em casos de risco.
Na área de fiscalização, a agência pretende intensificar inspeções em importadoras, farmácias e clínicas, além de ampliar o monitoramento de eventos adversos por meio do sistema VigiMed.
O plano também prevê articulação com entidades médicas, órgãos de controle e agências internacionais, além de ações de comunicação para orientar a população sobre os riscos do uso indiscriminado.
Outro ponto é a ampliação da oferta de produtos regularizados. Atualmente, há 17 pedidos de registro de medicamentos dessa categoria em análise prioritária na agência. “Com a queda da patente da semaglutida, uma boa parte desses produtos estão vindo com novas opções e foram solicitados [os registros] para a Anvisa e nós estamos priorizando essa análise”, explicou Safatle.
A iniciativa inclui ainda a criação de um grupo de trabalho interno para acompanhar a implementação das medidas e avaliar continuamente os resultados.